Fázový diagram
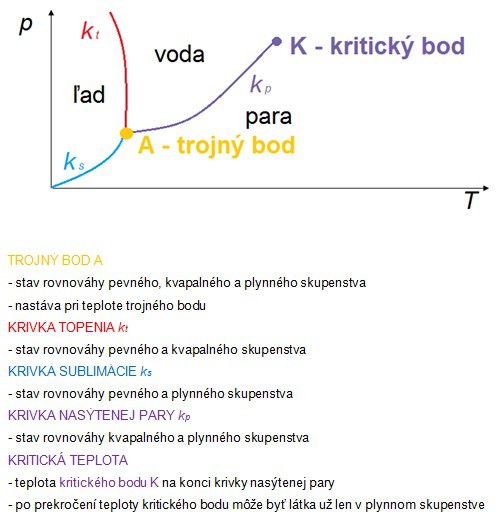
Každá látka sa topí, vrie, nadobúda rovnovážny stav pri vlastnej teplote za normálneho tlaku. Ak sa zmení tlak, zmena skupenstva a rovnovážne stavy medzi nimi nastávajú pri zmenených teplotách. Zaznamenávame ich do fázového diagramu, ktorý má vodorovnú os teplotnú (termodynamická teplota T [K]) a zvislú os tlakovú (p [Pa]). Pre jednotlivé látky môžeme zostaviť charakteristické fázové diagramy. Krivkami oddeľujeme oblasti pevného, kvapalného a plynného skupenstva.
Molekulová fyzika a termodynamika

